
دنیای علم و تکنولوژی
اخبار و مقالات مربوط به دنیای علم و تکنولوژی ترجمه شده از منابع معتبر
دنیای علم و تکنولوژی
اخبار و مقالات مربوط به دنیای علم و تکنولوژی ترجمه شده از منابع معتبردرباره من
دستهها
- تصاویر جالب علمی 60
- اخبار علمی 115
- تاریخ علم 21
- مقالات علمی 183
- حقایق علمی 29
- پرسش و پاسخ علمی 4
- تکنولوژی نظامی 170
- مشاهیر 10
- معرفی وبسایت علمی 10
- سخن بزرگان 4
- تفریح و سرگرمی 1
- شگفتیهای طبیعت 6
- مسابقه علمی 6
- زبان انگلیسی 18
- دیرین شناسی 34
- مهندسی مکانیک 56
- دنیای ریاضیات 51
- فایل های قابل دانلود 8
- پزشکی و سلامت 88
- ترین ها 36
- کنکور 1390 14
- نمونه سوال امتحانی و آزمون 20
- معرفی نرم افزار 4
- واژه نامههای تخصصی 1
- آزمایش های ساده و جالب فیزیک 4
- کنکور 13
- تکنولوژی نفت و حفاری 5
- بانک مقالات علمی 3
- آیرودینامیک و پرواز 6
- استانداردهای مهندسی 6
- محیط زیست 38
- باستان شناسی 5
- پروژه درسی و سمینار 5
- برنامه نویسی کامپیوتر 10
- رپرتاژ آگهی 1
ابر برجسب
جنگنده هواپیما ریاضیات ستاره زمین لرزه گرمایش جهانی F-35 سیاهچاله جنگ جهانی دوم موشک کنکور بمب افکن کرونا کووید 19 ویروسبرگهها
جدیدترین یادداشتها
همه- لئونارد اویلر
- بخشهای مختلف هواپیما و کارکرد آنها
- انسان بر لبه انقراض
- ساخت بزرگترین هواپیمای حامل پهباد توسط چین
- چرا تمامی اشکال حیات به اکسیژن وابسته هستند؟
- رایانش کوانتومی چیست؟
- فیلها: بزرگترین حیوانات خشکی
- کاربرد هوش مصنوعی در حل مسایل علمی با Deepseek
- اورکا فرمانروای اقیانوس
- روباتهای انسان نما
- تاریخچه ابداع و ساخت خودرو
- آخرین نئاندرتال
- مروری بر سبک های مختلف نقاشی
- نوآوری در حل تست های ریاضی
- بازی بزرگان: برزیل و فرانسه جام جهانی 1986
بایگانی
- تیر 1404 1
- خرداد 1404 3
- اردیبهشت 1404 1
- فروردین 1404 1
- اسفند 1403 1
- بهمن 1403 2
- دی 1403 1
- آذر 1403 1
- مهر 1403 1
- شهریور 1403 3
- مرداد 1403 1
- تیر 1403 3
- خرداد 1403 4
- اردیبهشت 1403 3
- فروردین 1403 2
- اسفند 1402 7
- بهمن 1402 2
- دی 1402 3
- آذر 1402 3
- آبان 1402 2
- مهر 1402 5
- شهریور 1402 4
- مرداد 1402 12
- تیر 1402 12
- خرداد 1402 5
- اردیبهشت 1402 6
- فروردین 1402 8
- اسفند 1401 6
- بهمن 1401 9
- دی 1401 2
- آذر 1401 3
- آبان 1401 1
- مهر 1401 1
- شهریور 1401 4
- مرداد 1401 7
- تیر 1401 12
- خرداد 1401 10
- اردیبهشت 1401 12
- فروردین 1401 4
- اسفند 1400 4
- بهمن 1400 7
- دی 1400 2
- آبان 1400 5
- مهر 1400 9
- شهریور 1400 1
- مرداد 1400 3
- تیر 1400 6
- خرداد 1400 7
- اردیبهشت 1400 8
- فروردین 1400 7
- اسفند 1399 12
- بهمن 1399 11
- دی 1399 1
- آذر 1399 7
- آبان 1399 2
- مهر 1399 1
- اردیبهشت 1399 7
- فروردین 1399 33
- اسفند 1398 13
- بهمن 1398 9
- دی 1398 1
- خرداد 1398 4
- اردیبهشت 1398 7
- بهمن 1397 5
- دی 1397 5
- آذر 1397 2
- آبان 1397 3
- مهر 1397 3
- شهریور 1397 1
- مرداد 1397 7
- تیر 1397 7
- خرداد 1397 2
- اردیبهشت 1397 6
- اسفند 1396 3
- بهمن 1396 5
- دی 1396 4
- آذر 1396 8
- آبان 1396 6
- مهر 1396 5
- شهریور 1396 6
- مرداد 1396 10
- تیر 1396 9
- خرداد 1396 5
- اردیبهشت 1396 3
- فروردین 1396 8
- اسفند 1395 3
- بهمن 1395 3
- دی 1395 1
- آذر 1395 4
- آبان 1395 2
- مهر 1395 7
- شهریور 1395 5
- مرداد 1395 1
- تیر 1395 3
- خرداد 1395 1
- اردیبهشت 1395 1
- فروردین 1395 3
- اسفند 1394 8
- بهمن 1394 2
- دی 1394 1
- آذر 1394 3
- آبان 1394 2
- مهر 1394 1
- مرداد 1394 1
- تیر 1394 2
- فروردین 1394 1
- اسفند 1393 4
- بهمن 1393 2
- دی 1393 1
- آبان 1393 1
- شهریور 1393 1
- مرداد 1393 1
- تیر 1393 3
- اردیبهشت 1393 7
- فروردین 1393 1
- اسفند 1392 2
- بهمن 1392 8
- دی 1392 6
- آذر 1392 16
- آبان 1392 14
- مهر 1392 19
- شهریور 1392 17
- مرداد 1392 6
- تیر 1392 2
- خرداد 1392 5
- اردیبهشت 1392 9
- فروردین 1392 1
- اسفند 1391 5
- بهمن 1391 8
- دی 1391 6
- آذر 1391 8
- آبان 1391 5
- مهر 1391 12
- شهریور 1391 7
- مرداد 1391 2
- تیر 1391 6
- خرداد 1391 7
- اردیبهشت 1391 8
- فروردین 1391 13
- اسفند 1390 7
- بهمن 1390 6
- دی 1390 11
- آذر 1390 2
- آبان 1390 6
- مهر 1390 4
- شهریور 1390 5
- مرداد 1390 8
- تیر 1390 15
- خرداد 1390 25
- اردیبهشت 1390 11
- فروردین 1390 1
- اسفند 1389 13
- بهمن 1389 12
- دی 1389 5
- آذر 1389 3
- آبان 1389 6
- مهر 1389 7
- شهریور 1389 6
- خرداد 1389 1
- اردیبهشت 1389 3
- اسفند 1388 7
- بهمن 1388 10
- دی 1388 11
- آذر 1388 7
- آبان 1388 17
- آذر 1387 1
- آبان 1387 9
- مهر 1387 5
- شهریور 1387 1
- مرداد 1387 3
- تیر 1387 7
- خرداد 1387 5
- اردیبهشت 1387 1
- فروردین 1387 3
- اسفند 1386 3
- بهمن 1386 9
- دی 1386 19
- آذر 1386 19
- آبان 1386 7
تقویم
تیر 1404| ش | ی | د | س | چ | پ | ج |
| 1 | 2 | 3 | 4 | 5 | 6 | |
| 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 21 | 22 | 23 | 24 | 25 | 26 | 27 |
| 28 | 29 | 30 | 31 |
جستجو
عناصر شگفت انگیز
یک عنصر ماده ای است که مولکول آن تنها از یکنوع اتم تشکیل شده است. عناصر ساده ترین شکل ماده بی جان بشمار می روند. گرچه جهان از بی شمار نوع ماده مرکب ساخته شده اما آجرهای ساختمانی آنها همین عناصر هستند که تعداد آنها محدود و در حدود 103 عدد است. از این تعداد تقریبا از عنصر 93 به بعد بسیار ناپایدار محسوب می شوند و طول عمر ناچیزی دارند.
بهترین روش طبقه بندی عناصر توسط دیمیتری ایوانیچ مندلیف دانشمند روسی در سال کشف شد که به نام جدول تناوبی موسوم گشت. در این جدول عناصری که دریک ستون قرار می گیرند ساختار الکترونی و خواص مشابهی دارند. از این گذشته بعدها معلوم گشت جدول تناوبی ساختار شگفت انگیز دیگری نیز دارد و اطلاعات بسیاری در مورد روند تغییر کمیت های فیزیکی مربوط به عناصر از آن می توان استخراج کرد.
جدول زیر فراوانی برخی عناصر مهم را در کل جهان هستی نشان می دهد. چنانچه دیده می شود هیدروژن و هلیوم فراوانترین عناصر هستند و تقریبا بیشتر پیکره ستارگان از این دو عنصر ساخته شده است (جداول این مقاله از کتاب علم مواد Brian S Mitchell اقتباس شده است).
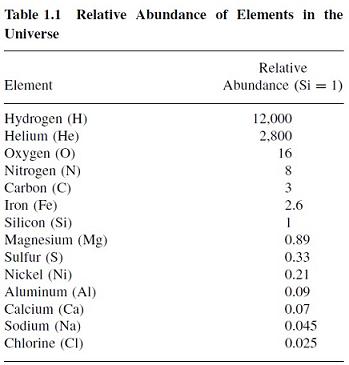
اما در پوسته زمین اوضاع کاملا فرق می کند و اکسیژن مقام اول را به خود اختصاص می دهد بطوریکه تقریبا نیمی از اتمهای سازنده پوسته زمین اکسیژن هستند. هلیوم یکی از آخرین مکانها را به خود اختصای می دهد به همین دلیل استخراج هلیوم از پوسته زمین تقریبا غیر ممکن است.
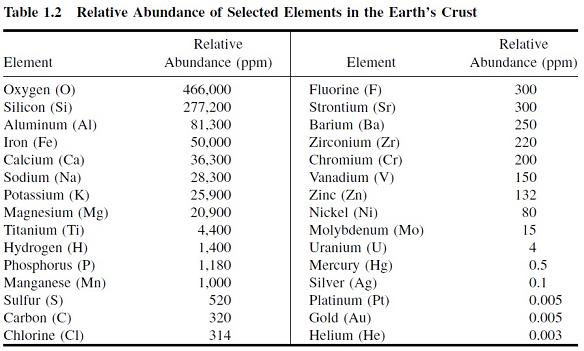
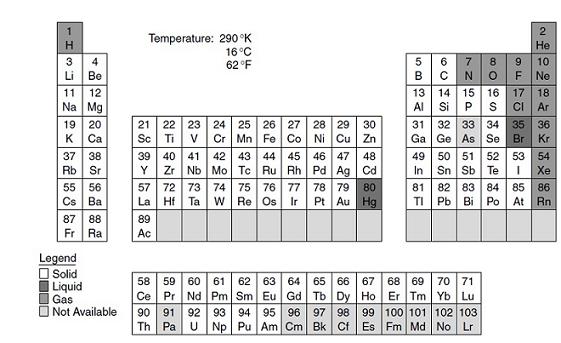
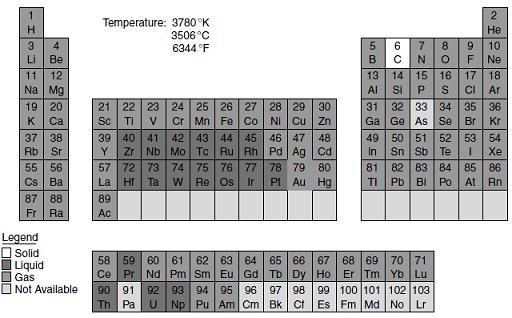
در غیاب اکسیژن، در دمای 16 درجه سانتی گراد بیشتر عناصر جامدند (جدول زیر) اما در دمای 3506 درجه سانتی گراد تنها کربن می تواند حالت جامد خود را حفظ کند و بسیاری از عناصر حتی آهن و روی نیز به شکل گازی درآمده اند (جدول زیر و دورتر).
یک آزمایش جالب در شیمی: خمیر دندان فیل
ترجمه و گردآوری: اصغر ناصری
یک استوانه مدرج بزرگ (مثلا 500 میلی متری) برداشته و حدود 50 میلی لیتر پروکساید هیدروژن 30 درصد در آن بریزید. به اندازه یک سرنگ مایع ظرفشویی به آن اضافه کنید. استوانه مدرج را روی یک سینی بزرگ قرار دهید. یک فنجان چای خوری پودر یدید پتاسیوم به آن بیافزایید و عقب بایستید. تصویر متحرک زیر نتیجه را نشان می دهد (تا باز شدن تمامی فریم ها صبر کنید).

چه اتفاقی افتاده است؟ واکنش زیر این تجزیه شیمیایی را فرموله می کند:
2 H2O2(aq) 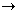 O2(aq) + 2 H2O(aq)
O2(aq) + 2 H2O(aq)
در حقیقت شما با واکنش تسریع شده تجزیه پروکساید هیدروژن به اکسیژن و آب سر و کار دارید. ستونی از کف و حبابهای اکسیژن از استوانه بیرون می زند. درست مانند خمیر دندانی که از لوله بیرون بزند.
پس یدید پتاسیوم در واکنش بالا چه نقشی دارد؟ یدید پتاسیوم نقش کاتالیزور را دارد و در تجزیه شیمیایی بالا وارد نمی شود.
این آزمایش کمی خطرناک است. پروکساید هیدروژن 30 درصد می تواند سوزاننده باشد. بنابراین از عینک و دستکش استفاده کنید.
منبع:
http://antoine.frostburg.edu/chem/senese/101/redox/faq/elephants-toothpaste.shtml